Onderwerp:
- Corrosie en roest
- Roest bestrijden
- Rost voorkomen
- Putcorrosie
- Contactcorrosie
Corrosie en roest:
De begrippen corrosie en roest hebben een nauw verwantschap met elkaar. Roest is het resultaat van corrosie. Deze twee begrippen worden echter vaak door elkaar gebruikt.
- Corrosie is een overkoepelende benaming van het aantasten van materiaal, door (chemische) reactie met hun omgeving;
- Roest ontstaat aan het oppervlakte van ijzer of staal als gevolg van de aanraking met water en zuurstof. Met roest wordt het oxideren van ijzer bedoelt, wat tevens een vorm van corrosie is.
Zodra metalen blootgesteld worden aan de normale atmosfeer (de buitenlucht) zal dit metaal een chemische verbinding aan gaan met zuurstof. In dit geval gaat het metaal roesten. Roest is te herkennen aan de roodbruine laag dat op het metaal verschijnt en ontstaat wanneer ijzer reageert met zuurstof, in aanwezigheid vocht uit de buitenlucht of water. Het is een vermenging van ijzeroxide- en en ijzerhydroxide. Roest ontwikkelt zich steeds verder en kan metaal volledig wegvreten. Na verloop van tijd is al het ijzer omgezet in roest en verliest daarmee zijn gunstige eigenschappen.
In het geval ijzer wordt blootgesteld aan zuurstof en water, zullen na verloop van tijd zuurstof en ijzer zich op atomair niveau gaan hechten. Er ontstaat hierdoor een nieuwe verbinding: ijzeroxide. Water versnelt het gehele proces doordat water fungeert als katalysator. De kleine watermoleculen dringen door in het metaal en vormen nog meer zuren, waardoor metaal nog meer wordt blootgesteld aan de oxidevorming. Het roesten gaat nog sneller in zeewater door de hogere concentratie aan natriumchloride-ionen.
Onder de autolak kunnen er roestplekken ontstaan. Dit komt doordat de lak ook min of meer poreus is en daardoor vocht en zuurstof door kan laten. Om de laklaag dicht te houden, is het goed om de auto regelmatig in de was te zetten. Vooral in de winter, met veel vochtige omstandigheden en pekel, is dit laatste een goede manier om roest zo veel mogelijk tegen te gaan.
Wanneer er diepe krassen of steenslag aanwezig is, dan is op deze plek de beschermende laklaag weg en kan het er om heen ook gaan roesten. Het is daarom verstandig deze plekjes zo snel mogelijk bij te werken met een lakstift, of opnieuw te laten spuiten.
In de afbeelding hiernaast zien we een VW Beetle met roestige carrosseriedelen. Dit voertuig valt onder de noemer “Rat rod”. Voertuigen die als Rad rot zijn omgebouwd, bestaan uit opzettelijk versleten en ongespoten delen (in dit geval roest) en afgedankte onderdelen.

In zeer weinig gevallen kan men roest waarderen. Toch krijgt ieder voertuig er vroeg of laat mee te maken. Naast het vochtige klimaat in Nederland, heeft de pekel op het wegdek in de winter een verhoogde kans op roest. Naast de cosmetische delen, kunnen ook delen van het chassis of carrosserie worden aangetast. Op langere termijn kan dit leiden tot een onveilig voertuig en tot afkeur tijdens de APK.
Autofabrikanten trachten de materialen in en om de auto zoveel mogelijk roestbestendig te maken. Dit zijn een aantal van de roestwerende behandelingen:
- verzinken van de carrosserie;
- wax-behandelingen toepassen;
- primer- en grondlaklagen aanbrengen;
- hoogwaardige laklagen aanbrengen.



Roest bestrijden:
Roest ontstaat doordat ijzer zich heeft verbonden met zuurstof. Het is onjuist door te denken dat roest te bestrijden is door te zorgen dat er geen zuurstof meer bij het ijzer komt. Staal is geen homogene stof, maar een mix van materialen die bij recycling worden samengebracht, bijvoorbeeld oude autowrakken. In het staal bevinden zich ook andere metalen. Tussen de kristallen van twee verschillende materialen heerst een klein spanningsverschil, waarin een geleidende vloeistof voor contact tussen de kristallen kan zorgen. Het daaruit ontstane elektrische stroompje zorgt ervoor dat het minst edele metaal in oplossing gaat. Vloeit er bijvoorbeeld een stroom tussen ijzer en koper, dan lost het ijzer op. De opgeloste ijzerdeeltjes verbinden zich met zuurstof. Met de kleinste hoeveelheid water in de carrosserielaag, al is het slechts één watermolecuul, wordt het proces in stand gehouden.
Wanneer men last heeft van roest onder de lak heeft het geen zin om over roest heen te spuiten. De roest vreet onder de laklaag onverminderd verder. Omdat het volume van rost groter is dan het staal, zal op ten duur de laklaag barsten. Daardoor ontstaat er een opening waar extra water kan indringen en het roestproces versnelt. Om roest te bestrijden, wordt staal ontroest door het oppervlak te stralen. Vervolgens wordt er zo snel mogelijk een roestwerende primerlaag aangebracht. Hiermee mag men niet te lang wachten, omdat het vocht uit de buitenlucht zich anders aan de ijzerdeeltjes bindt.

Roest vormt zich onder de laklaag. Beginnende roest is daarom niet altijd makkelijk te herkennen. In de onderstaande vier afbeeldingen is een kokerbalk van een VW Golf IV te zien waar het roestige metaal is weggeslepen. Voordat eraan werd begonnen, was er alleen nog sprake van loslatende bitumen op de rand onder de dorpel. De kokerbalken vertoonden geen oneffenheden. Bij het weghalen van de bitumen werden de bruine randen zichtbaar. Het metaal hieromheen was al in die mate aangetast, dat het gemakkelijk afbrak. De foto’s tonen hoe roest zich onder bitumen kan gedragen.




Roest voorkomen:
In de eerste paragraaf werd in de opsomming van maatregelen om roesten te voorkomen het “verzinken” genoemd. Fabrikanten brengen tijdens de productie van de auto een dun laagje zink aan. Dit biedt de zogenaamde kathodische bescherming. Omdat vanuit zink eerder elektronen zullen ontsnappen, lost het zink eerder op dan het ijzer. Zink gaat gemakkelijker een verbinding aan met de zuurstof in de lucht. Het zink is vrij hard en vormt een afsluitende laag. Bij diepe krassen door de lak- en zinklaag tot op het staal zal het staal nauwelijks reageren. Bij voldoende zink in de buurt, zal de elektrische stroom de goede kant op gaan. Om die reden biedt zink een langdurige bescherming tegen corrosie en roest.

Verzinkt staal heeft niet alleen voordelen. Door de toename hiervan neemt de hoeveelheid van het zuivere staal af. Producenten hebben zinkvrij staal nodig om o.a. motoronderdelen te maken. Zink heeft de eigenschap om bellen te vormen in het staal, met zwakke plekken tot gevolg.
Putcorrosie:
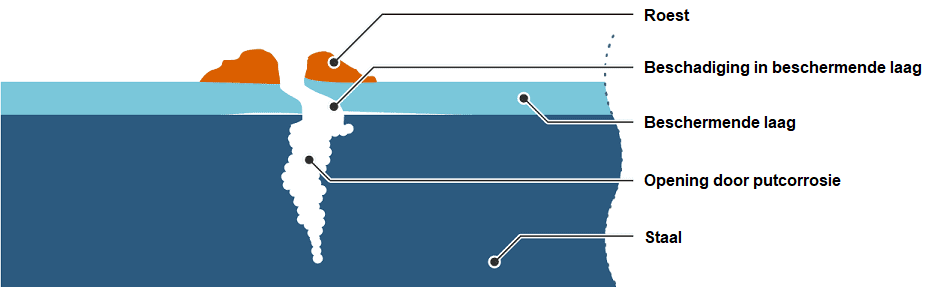
Putcorrosie (Engels: pitting) is een plaatselijke aantasting van het materiaaloppervlak. Putcorrosie treedt op bij materialen die zich middels een oxidelaag tegen corrosie beschermen en ontstaat voornamelijk op de plek waar deze oxidelaag is beschadigd. Putcorrosie vreet zich snel en diep in het materiaal. Dit is het gevaarlijkste, omdat het materiaal er ogenschijnlijk nog goed uitziet, en men onvoldoende de diepte van de corrosie kan zien.
De onderstaande afbeelding toont de dwarsdoorsnede van een stalen voorwerp met putcorrosie. Aan de bovenkant is slechts een kleine hoeveelheid roest te zien. Het “putje” in de roest verraad de opening die in het staal is ontstaan.
Putcorrosie kunnen we tegenkomen in o.a. remleidingen. Op het moment dat de opening dieper wordt, bestaat de kans dat de remvloeistof daardoor naar buiten kan lekken.

Contactcorrosie:
Dit treedt op wanneer twee verschillende metalen met elkaar in nauw contact komen. Er wordt een spanningsverschil opgewekt tussen deze twee metalen, waarbij er een reactie ontstaat. Dit zien we als er bijvoorbeeld een edelstaalschroef aan een verzinkte staalplaat wordt vastgeschroefd. Het edelere metaal werkt de corrosie in de hand en gaat daardoor roesten. Dit noemt men contactcorrosie.
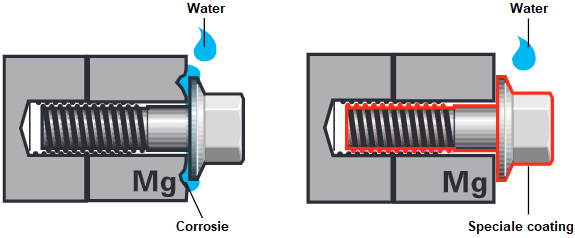
In de volgende afbeelding worden twee voorbeelden getoond van een magnesium component, bijvoorbeeld een versnellingsbak, welke is bevestigd met een bout die is gemaakt van een ijzerlegering. Als het contactoppervlak wordt blootgesteld aan water, ontstaat er een elektrische stroom tussen de twee metalen en leidt dit tot contactcorrosie. Tegelijkertijd wordt het magnesium afgebroken. Contactcorrosie kan worden voorkomen door de elektrische stroom tussen de twee metalen te remmen door de bout met een niet-geleidende, dus isolerende laag te coaten.
De onderstaande tabel toont de verschillende combinaties van materialen (van bijvoorbeeld motoronderdelen of de behuizing van de versnellingsbak) en wat de keuze voor de materialen van de bout of schroef voor invloed heeft op de contactcorrosie.

